Management of Asthma and COPD Exacerbations in Adults in the ICU
- https://doi.org/10.1016/j.chstcc.2024.100107
- CHEST Critical Care 2024
ICUにおける管理についてレビューがありましたのでまとめます!
Key points
- コルチコステロイド
- 喘息急性増悪には、プレドニゾロン40~50 mg/日(または同等薬)を5~7日間使用。
- COPD急性増悪では5日間の使用が推奨される。
- メチルプレドニゾロン240 mg/日を超える高用量は治療失敗や感染リスクを高めるため避けるべき。
- 非侵襲的換気(NIV)
- COPD急性増悪の初期治療法として推奨。
- 喘息急性増悪では慎重に適用する必要がある。
- 侵襲的換気を必要とする患者のモニタリング
- 気道内圧(Pplat)および内因性呼気終末陽圧(PEEPi)を観察。
- Pplatは30 cm H2O以下を維持することが目標。
- NIVまたは高流量鼻カニュラ療法(HFNT)の使用
- COPD急性増悪後の抜管直後に使用することで再挿管のリスクを低減できる。
- 喘息急性増悪では明確な有効性は確認されていない。
- 体外式膜型人工肺(ECMO)の注意点
- 喘息またはCOPDの生命を脅かす急性増悪でECMOを開始した場合、最初の24時間に二酸化炭素分圧(PaCO2)を20 mmHg以上または治療前の50%以上削減しないよう注意する。神経学的合併症を回避するため。
評価
- 酸素飽和度(SpO₂)の評価
- パルスオキシメトリーを用いて酸素化と心拍数を評価。
- 動脈血ガス(ABG)検査
- 疲労感や傾眠、予測ピーク呼気流量(PEF)または一秒量(FEV₁)が50%未満の患者、またはその他の臨床的懸念がある患者に推奨される。
- 呼吸器ウイルス病原体の検査
- ウイルス感染を特定するための検査。
- 喀痰細菌培養
- 重症喘息やCOPD患者ではコロニー形成が見られる可能性があり、培養結果を慎重に解釈する必要がある。
- 胸部X線、心電図(ECG)、およびB型ナトリウム利尿ペプチド(BNP)測定
- 合併症や併存症の有無を評価するために推奨。
- 肺塞栓症(PE)の評価
- 臨床判断に基づき、Dダイマー検査やCT血管造影(CTA)を考慮。
重症の定義
喘息:呼吸数30回/分以上、心拍数120回/分以上、SpO₂90%未満(室内気で)、PEFが予測値の50%以下
COPD:呼吸数24回/分以上、心拍数95回/分以上、SpO₂92%未満、既知の酸素飽和度から3%以上の低下、急性高CO2血症(PaCO₂45 mmHg以上、pH7.35未満)
病態生理学的特徴
急性増悪時には、炎症反応が通常数日間にわたって進行し、微小血管の透過性亢進と気道の腫脹を引き起こす。さらに、喘息急性増悪でより顕著な特徴である気管支痙攣や、小気道内の粘液閉塞により気道抵抗が増加する。気道抵抗の増加は、呼気流制限によって悪化する可能性があり、これは弾性反跳の低下により気道が早期に閉鎖される現象である。この結果、喘息およびCOPD急性増悪における気流閉塞は換気/血流比(V/Q)の不均衡を引き起こし、呼気時間定数(潮気量の63%を排出するのに必要な時間、肺抵抗×コンプライアンスで算出)が増加する。
呼気時間定数が長くなると、肺胞圧が大気圧に戻るのを妨げ(つまり、呼吸サイクル全体で肺胞圧が陽圧のままになる)、頻呼吸の状況下でガス閉じ込めや動的過膨張を進行させる可能性がある(図1A参照)。動的過膨張により肺のコンプライアンスが低下し、圧-容量曲線の頂点付近で作動するようになり、また横隔膜が平坦化するため、その機械的効率が低下する。この結果、不利な長さ-張力関係が生じ、呼吸筋の作業量が増加する。最終的には、この機械的な不利な状態が疲労と呼吸不全につながる可能性がある。
したがって、治療の主な目標は、気道炎症を抑制し、気管支痙攣を逆転させることにある。重症例では、気道炎症の改善を待つ間、非侵襲的または侵襲的な機械換気で呼吸筋の負担を軽減することが必要である。
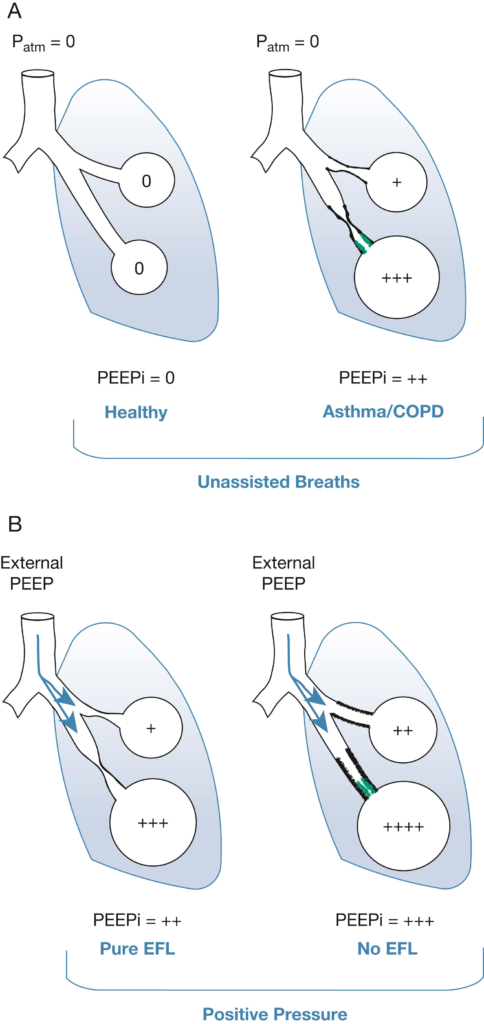
健康な成人では、呼気終末時に肺胞圧が大気圧(Patm)と均衡し、気流が停止する。しかし、重度の喘息またはCOPD急性増悪では、気道の炎症や気管支痙攣、一部の患者では弾性反跳の低下に起因する早期気道閉鎖(EFL)が発生し、呼気時間が延長する。この結果、肺胞圧がPatmに戻らず、呼気終末時に肺胞圧が陽圧のままとなり(PEEPi:内因性呼気終末陽圧)、異なる時間定数に基づく異質性を持つ肺ユニットがしばしば認められる。
B. 外部PEEP適用時の反応
外部PEEPの反応はEFLの存在に依存する
・純粋なEFLの場合
PEEPiの80%までの外部PEEPを適用しても、全体のPEEPまたは動的過膨張は変化しない。これは「ウォーターフォール効果」によって説明されry。この効果では、EFL内の臨界閉鎖部位の下流に圧力を適用しても、下流圧が臨界閉鎖圧と等しくなるまで、上流の圧力(PEEPi)や流れに影響を与えない。この現象は、滝の高さを超えない限り、滝の下流の川の水位が滝を流れ落ちる水流に影響を与えない状況に例えられる。
・EFLが存在しない場合
外部PEEPが肺胞に伝わり、PEEPiおよび動的過膨張が悪化する。外部PEEPに対する全体的なPEEPの逆説的な減少も記録されており、これはEFLと異質な肺によるものと考えられている。
治療
| 薬剤カテゴリ | 作用機序 | 喘息での使用 | COPDでの使用 | コメント |
|---|
| 短時間作用性β2作動薬(SABA) | 気管支拡張および平滑筋弛緩(気道β2受容体刺激) | 全患者対象: • MDI/DPI(スペーサー使用): アルブテロールを4~8吸入×20分ごとに3回、その後2~4吸入を1~4時間ごと • ネブライザー: アルブテロール2.5~5 mgを20分ごとに3回、その後2.5~5 mgを1~4時間ごと | 全患者対象: • MDI/DPI(スペーサー使用): アルブテロールを4吸入×1時間ごとに3回、その後2~4吸入を2~4時間ごと • ネブライザー: アルブテロール2.5 mgを1時間ごとに3回、その後2.5 mgを2~4時間ごと | ・アルブテロールとレバルブテロールの効果と安全性は同等だが、アルブテロールがfirst line。 ・MDI/DPI with spacerとネブライザーは効果同等だが、重症患者にはネブライザーが推奨 ・COPDでは過酸素を避けるため酸素ではなく空気で駆動するネブライザーが推奨 ・安定後は吸入器へ切り替え早期退院を促進 |
| 短時間作用性抗コリン薬(SAMA) | ムスカリン性アセチルコリン受容体の阻害による気管支拡張 | 全患者対象: • MDI(スペーサー使用): イプラトロピウム17 μg/吸入を4~8吸入×20分ごとに3回、その後1~4時間ごと • ネブライザー: イプラトロピウム0.5 mgを20分ごとに3回、その後1~4時間ごと | 全患者対象: • MDI(スペーサー使用): イプラトロピウム17 μg/吸入を2~4吸入×1時間ごとに最大3回、その後2~4時間ごと • ネブライザー: イプラトロピウム0.5 mgを1時間ごとに最大3回、その後2~4時間ごと | ・MDI/DPI with spacerとネブライザーの効果は同等だが、重症患者にはネブライザーが推奨 ・COPDでは過酸素を避けるため酸素ではなく空気で駆動するネブライザーが推奨 ・安定後は吸入器へ切り替え早期退院を促進 |
| コルチコステロイド | 炎症性メディエーター抑制、好酸球の誘導抑制とアポトーシス誘発 | 全患者対象: プレドニゾロン1 mg/kg/日(最大50 mg/日)または同等薬を5~7日間投与 | 全患者対象: プレドニゾロン40 mg/日または同等薬を5日間投与 | ・非常に高用量(メチルプレドニゾロン240 mg/日超)は避けるべき ・主にグルココルチコイド作用を持つコルチコステロイド(例:プレドニゾロンやメチルプレドニゾロン)は、ミネラルコルチコイド作用を持つもの(例:ヒドロコルチゾンやデキサメタゾン)よりも広く研究されているため、一般的に優先されるが、いずれの製剤も使用可能。 ・経口投与が迅速かつ低コストで推奨 |
| 抗生物質 | 細菌感染の抑制(核酸、タンパク質、細胞壁の合成阻害) | 細菌感染の懸念がある場合: アモキシシリン/クラブラン酸、マクロライド、テトラサイクリン、または肺炎をカバーする同等薬を5~7日間投与 | 息切れ、痰量、痰の膿性がすべて増加、または膿性痰を含む2つの症状がある場合、またはNIV/IMVが必要な患者: アモキシシリン/クラブラン酸、マクロライド、またはテトラサイクリンを5~7日間投与 | ・緑膿菌のリスクがある場合(慢性コロニー形成、FEV1 <50%、気管支拡張症、慢性ステロイド使用)、抗緑膿菌薬を検討 |
| 静脈内マグネシウム | 平滑筋のカルシウムチャネル抑制と副交感神経遮断 | 初期治療に反応しない場合: 2 gを20分間で投与 | 初期治療に反応しない場合: 2 gを20分間で投与 | ・喘息およびCOPDで入院率を低下させる可能性 ・SABAの効果を増強させるかも ・重症患者へのデータは限られている |
| 静脈内ケタミン | NMDA受容体非依存の気管支拡張 | ケースバイケースで使用: 0.2-0.5 mg/kgの静脈内投与、その後0.05-0.25 mg/kg/時の持続投与 | 推奨されない | ・喘息増悪に関するデータは限定的 ・呼吸抑制リスクがあるため非挿管患者は厳密に監視する必要がある ・IMVを受けている患者には、より高用量(0.5~2 mg/kg/時)を検討 |
| ヘリウム-酸素混合ガス | 密度低下による気道抵抗の低下と呼吸仕事量の軽減 | ケースバイケースで使用: 70%-80%ヘリウム+20%-30%酸素の混合気体 | ケースバイケースで使用: 左記と同じく | ・喘息では最も重度の肺機能障害患者において改善効果が見られる ・COPDではNIV失敗率の減少傾向あり |
| 揮発性麻酔薬 | 平滑筋弛緩による気管支拡張(複数の異なる機構が関与すると考えられる) | セボフルラン: 1.4%-2.6% デスフルラン: 2.5%-8.5% イソフルラン: 1.0%-3.0% | 使用は推奨されない(データ不足および効果が確認されていないため)。 | ・喘息急性増悪における前向きデータは非常に限られているが、呼吸力学の改善が見られる可能性がある。 ・COPD急性増悪に関する研究では、静脈内鎮静と比較して呼吸力学に対する効果が混在した結果となっている。 |
| 生物製剤 | IgEまたはIL-5の阻害による炎症抑制 | ケースバイケースで使用: オマリズマブ150-375 mg、メポリズマブ100 mg、ベンラリズマブ30 mgを皮下注 | 推奨されない | ・喘息増悪における使用は主にケースレポートに限定 ・最新の生物製剤(デュピルマブなど)の効果は不明 |
メチルキサンチン類(例:テオフィリンやアミノフィリン)およびテレブタリン(静脈内β2作動薬)は、吸入性β2作動薬と比較して効果が劣るため、成人の喘息やCOPD急性増悪には推奨されていない。また、メチルキサンチン類は、頻脈性不整脈などの副作用や有害事象のリスク増加と関連している。
★NIVについて
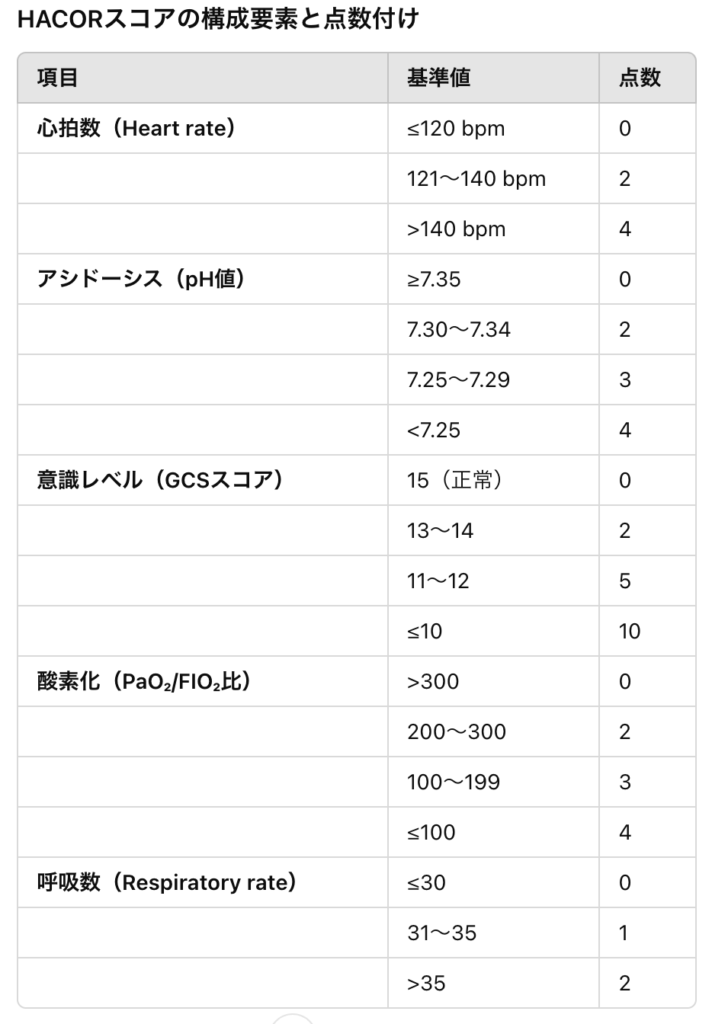
COPDにおける有用性は示されている(挿管必要性減少、死亡率短縮、ICUおよび病院滞在期間短縮など)。ただし、20%程度はNIV治療失敗となり挿管管理となりうる(リスクは、高齢、BMI高値、APACHEⅡスコア高値、NIV使用しても持続する低酸素/高CO2血症)。COPD患者におけるNIV失敗予測としてHACORスコアが使用されることがある。

喘息急性増悪におけるNIVの役割は明確には定義されておらず、Global Initiative for Asthma(GINA)のガイドラインでもその使用についての推奨は示されていない。
ただし、少数の小規模RCTでは、NIVが肺機能パラメータを改善し、ICUおよび病院滞在期間を短縮することが示されている。また、5万3,000人以上の参加者を含む後ろ向き研究では、NIVが死亡率の低下および侵襲的換気(IMV)の必要性の軽減と関連していることが報告されている。喘息に対するNIVの使用は過去数十年間で増加しており、IMVの使用が減少する一方で、死亡率や病院滞在期間に変化は見られていない。
→ICUで管理されるほとんどの重症喘息急性増悪患者に対して、慎重にNIVを試みることができると思われるが、生命を脅かす急性増悪を伴う患者では注意が必要である。
★IMVについて
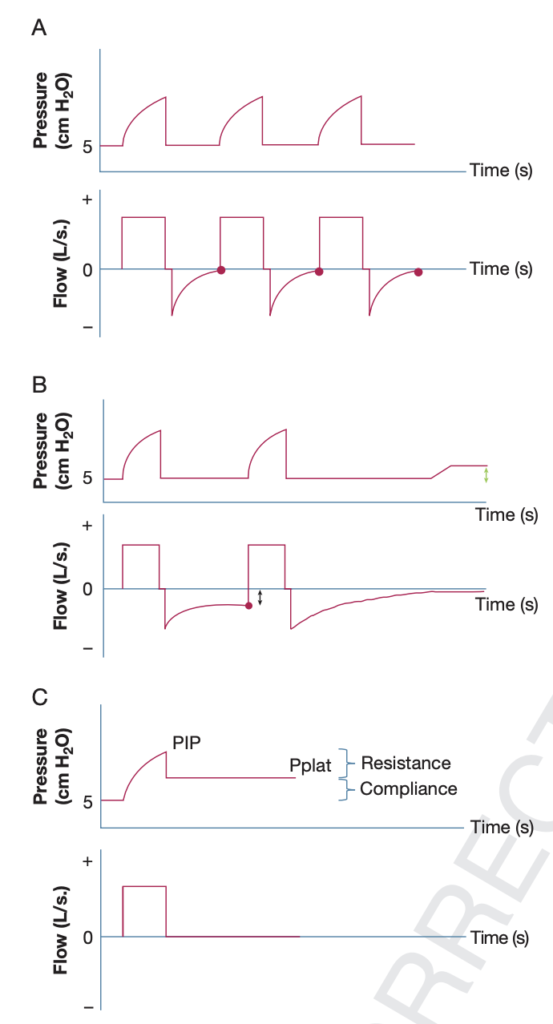
・Ppltは30以下で管理
・内因性PEEP(PEEPi)の存在を波形から感じ取る
これが重要です。
Bの図では呼気ホールドを使うことで設定したPEEPより上昇していることがわかります(PEEPiの存在)。もちろん呼気終了時点でFlowが基線に戻っていないことでも判断できますね。
→これがあるときは、吸気時間短くして呼吸数減らす(呼気時間伸ばす)、換気量減らす、が必要。
酸素療法、HFNT、NIV、IMV、VV ECMOの適応、初期設定、合併症
| 治療法 | 適応 | 初期設定 | 合併症 |
|---|---|---|---|
| 酸素療法(Supplemental O₂) | 喘息:SpO₂ < 92% COPD:SpO₂ < 88% | 流量:1~15 L/分で調整 目標SpO₂:喘息で93~95%、COPDで88~92% | COPDでの高酸素血症は死亡率増加に関連 鼻出血 |
| 高流量鼻カニュラ酸素療法(HFNT) | 呼吸困難(例:補助呼吸筋の使用)酸素投与にもかかわらず低酸素血症が持続 | 流量:15~60 L/分PEEP:3~5 cm H₂O(必要に応じて高流量で設定)目標SpO₂:喘息で93~95%、COPDで88~92% | 閉所恐怖症、不快感 嚥下機能障害や誤嚥のリスク |
| 非侵襲的換気(NIV) | 呼吸困難酸素投与にもかかわらず低酸素血症が持続PaCO₂ ≥ 45 mmHgかつpH ≤ 7.35 | 圧力支持を調整し、目標VT:6~8 mL/kg(理想体重)初期PEEP:約5 cm H₂O目標SpO₂:喘息で93~95%、COPDで88~92% I:E比:1:2~1:4 | 閉所恐怖症、不快感 マスク接触部の皮膚損傷胃拡張や誤嚥のリスク |
| 侵襲的機械換気(IMV) | 心停止または血行動態の不安定性NIVに耐えられない、またはNIV失敗による呼吸不全の悪化意識障害大量の誤嚥または持続的な嘔吐 | VT:6~8 mL/kgRR:10~12回/分PEEP:0~10 cm H₂OI:E比:1:2~1:4吸気流量:60~100 L/分 | バロトラウマ(例:気胸)人工呼吸器関連肺炎 気管チューブ関連合併症(例:気管狭窄) 筋力低下 |
| 静脈-静脈型ECMO(VV ECMO) | pH < 7.25を伴う高炭酸ガス性呼吸不全IMVによる最適治療にもかかわらず低酸素血症が持続過膨張による血行動態の不安定性 | 流量:2~6 L/分(目標SpO₂に合わせて調整)FDO₂:目標SpO₂に合わせて調整初期24時間でPaCO₂を20 mmHg以下に減少を目標 | 出血 血栓症 感染症 カニューレ挿入に伴う合併症(例:血管損傷) |
★VVECMOについて
スイープガス流量を調整して、PaCO₂をゆっくり正常化する(24時間以内にPaCO₂が20 mmHg以上、または50%以上急激に低下すると、脳卒中/脳出血などの神経学的合併症のリスクが増加する)。
肺保護のため、ARDSで使用されるような肺保護戦略(Pplt25以下、PEEP5-10、RR4-15など)がとられることもある。
抜管
COPD患者ではNIVやHFNCの使用により死亡率低下、再挿管率低下、が認められているが、喘息患者では不明。抜管後、再挿管リスクが高い人はNIVの方が良さそう。
まとめ
重症喘息、COPD急性増悪についての呼吸管理戦略についてのまとめでした。
ステロイドや抗生剤から、NIV、HFNC、IMVまでの一連の流れとして覚えておきたいですね。









コメント