Advances in management of heart failure
- BMJ 2024; 385 :e077025
- doi:10.1136/bmj-2023-077025
心不全についてのレビューがBMJから出ていましたのでまとめます。
心不全の予防
未治療の高血圧は心不全の一般的な原因である。血圧を最適にコントロールすると、心不全の発症が40%減少する。
DMがあるCKD患者では、SGLT2iとフィネレノンの両方が心不全発症リスクを軽減する。
HFpEFの診断
HFpEFの定義のほとんどでは、弁疾患、不整脈、心膜拘束、高心拍出による心不全症状のある患者は除外されている。心臓カテーテル法による侵襲的検査は左室充満圧の上昇を判定する上でのゴールドスタンダードであるが、非侵襲的に診断することも可能。しかしながら単一の検査で、高い感度・特異度を示すものはない。
以下のFigは、左室拡張末期圧の上昇を検査する一般的な非侵襲性検査の検査特性であるが、感度と特異度の両方が 70% を超える検査はない。
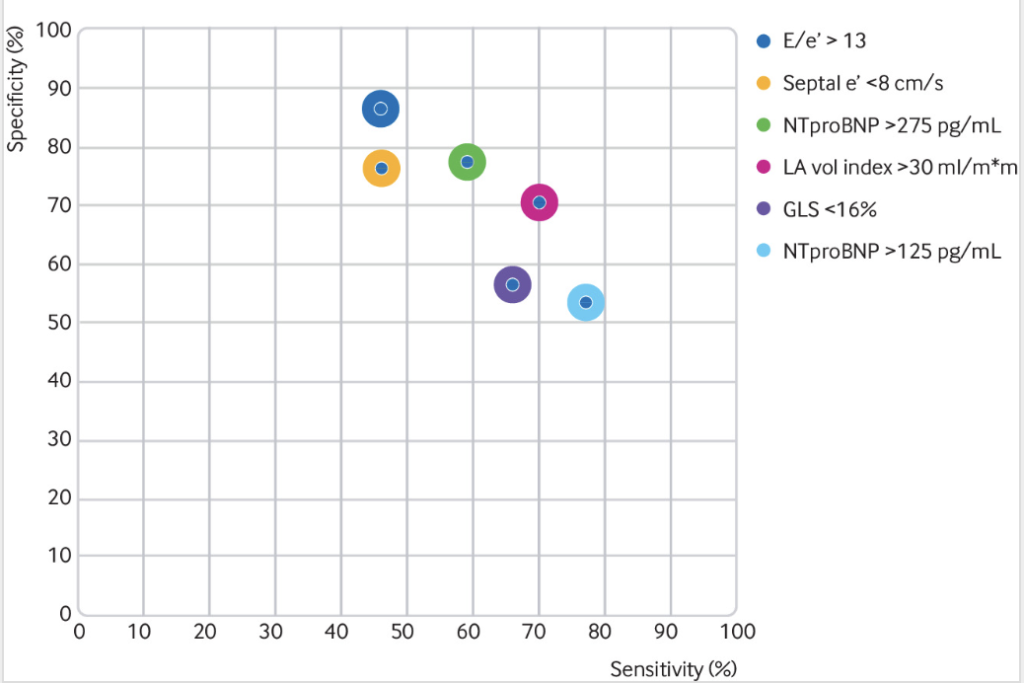
心不全症状の根本的な原因を特定することは、診断後の重要な第2ステップである。心エコー検査以外の追加検査が必要になることが多く、心臓磁気共鳴(CMR)画像による定期的なスクリーニングは必ずしも有用とは言えないが、選択的に使用すると、多くの場合有用な情報が得られる。DCMの患者や心エコー検査で著しい肥大が認められる患者は、CMR の恩恵を最も受けやすいと考えられる。
ガドリニウムによる後期増強のパターンと特定のT1およびT2技術は、心筋梗塞、心筋炎、シャーガス病、アミロイドーシス、鉄過剰症、サルコイドーシス、ファブリー病を含む浸潤性心筋症の診断を示唆する場合がある。
HFrEFに対する4つの薬物治療の柱
HFrEFの場合、生存率を改善する薬剤が現在4種類ある。
- ACE/ARB/ARNI
- βB
- MRA
- SGLT2i
4つの柱を組み合わせることで、治療を行わない場合と比較して、死亡率の相対リスクが73%減少し、NNT4である。
どの薬剤から開始するか、についてはまだ確認されたエビデンスは乏しいが、SGLT2iとMRAから始めるというものや、4剤を少量から同時に始める、というものもある。
以下のFigはHFrEFの治療概要である。
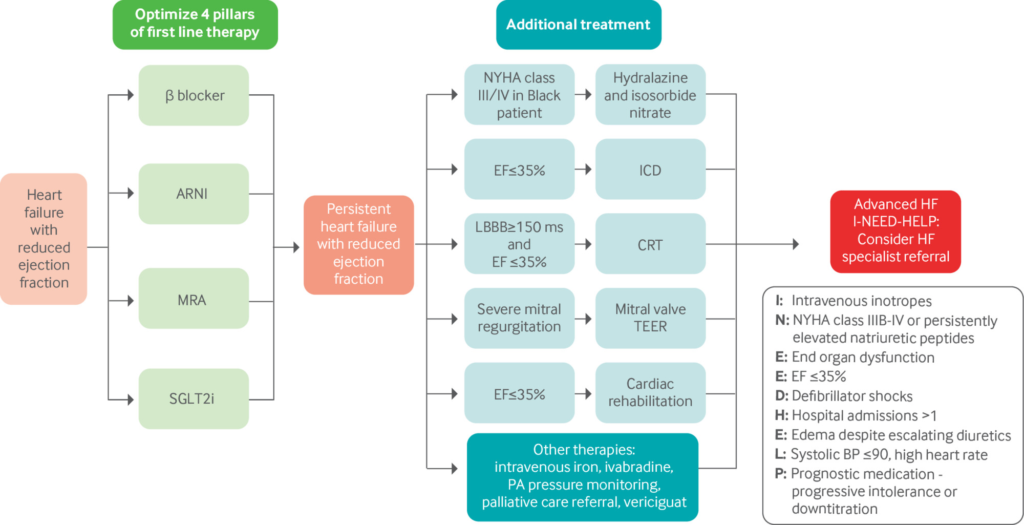
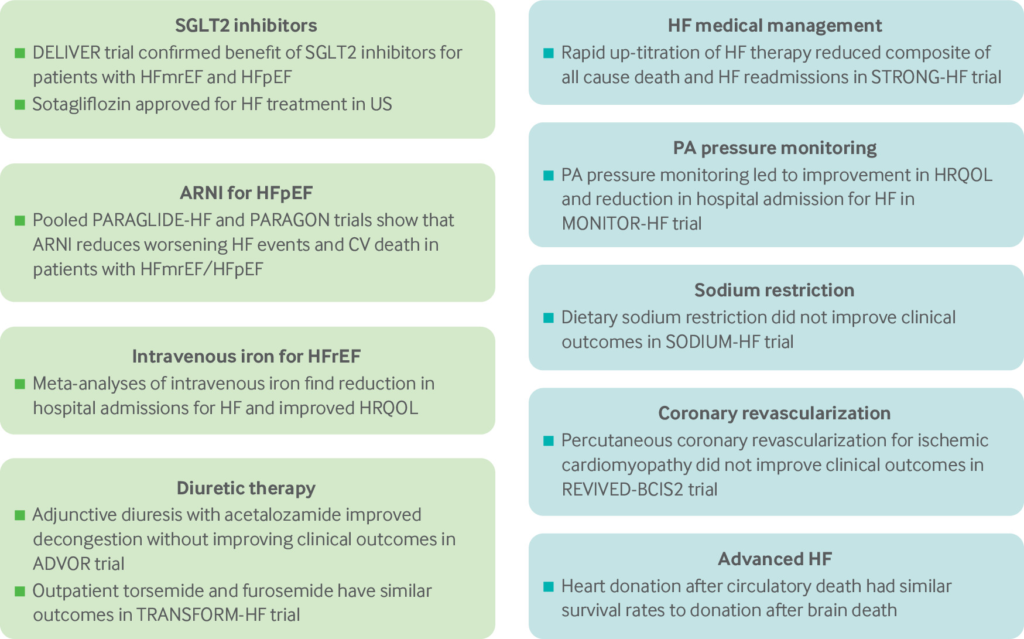
<ARNI>
PARADIGM-HF trialでは、サクビトリルとバルサルタンを併用した場合、エナラプリルと比較して、心血管疾患による死亡または心不全による入院が20%減少した (HR 0.80、95% CI 0.73~0.87)。
PIONEER-HF trialでは、入院中にサクビトリル/バルサルタンを開始した患者は、エナラプリルで治療した患者と比較して、NT-proBNP濃度が低下した (変化率 0.71、95% CI 0.63 ~ 0.81)。
ACEiと併用したARNIの使用は禁忌である。
NYHA class IV症状と定義される進行性心不全患者、または慢性の強心療法を受けている患者では、ARNIによる利点は認められない。
<SGLT2i>
糖尿病が既往にあり、最近心不全で入院した1222人の患者を対象とした研究では、ソタグリフロジンを退院前または退院直後に開始すると、プラセボと比較して、心血管疾患による死亡、心不全による入院および緊急受診が減少した (HR 0.67、0.52 ~ 0.84)。
SCORED trialでは、糖尿病と腎機能障害を患う10584人の患者(うち20%が心不全)をソタグリフロジンまたはプラセボに無作為に割り付けた。心血管死、心不全による入院、心不全による緊急受診の複合エンドポイントはソタグリフロジンによって減少し、心不全のある患者とない患者で同様の効果が得られた(HR 0.74、0.63~0.88)。
DAPA-HF trialでは、ダパグリフロジンにランダム化されてから28日目までに、プラセボと比較して心血管死または心不全の悪化が有意に減少した(HR0.51、95%CI 0.28~0.94)。臨床的な有用性があらわれるまでの時間はかなり早い。
さらに、SOLOIST-WHF trialでは、プラセボと比較してソタグリフロジンで治療された1222人の患者では、主要評価項目の持続的かつ有意な減少が現れるまでの時間は27日でありこちらも早期の有用性が示された (HR9.62、0.39~0.99)。
しかし、HFpEFの場合、臨床的有用性が現れるまでの時間は2倍長くなるという報告もあり。
<利尿薬>
利尿薬は鬱血の兆候や症状がある患者の治療の柱であるが、死亡率を改善することは示されていない。
ADVPR trialでは、静注ループ利尿薬に加えて静注アセタゾラミドを加えるとうっ血解除効果が強まる(3日以内のうっ血除去成功率: 42.2% vs 30.5%、P<0.001)。
HFrEF患者において、EFが改善した場合の治療
HFrEF患者で、EFが改善した患者でもHFrEF治療の継続が推奨されるが、症状が改善しEFが改善した後で用量増加や追加薬剤が必要かどうかは不明である。
HFmrEF、HFpEF患者の治療
SGLT2i(ダパグリフロジン(DELIVER trial)、エンパグリフロジン(EMPEROR-Preserved trial))はHFmrEF、HFpEFに対する第一選択薬として推奨されている。
HFrEFの他の治療法は、ARNI、ACE阻害薬、ARB、MRAよりも有益性がはるかに弱い。
β遮断薬はHFpEF患者には推奨されない。
EFと薬物治療によるメリット
β遮断薬の場合、LVEFが50%未満の場合に心血管疾患による死亡率の減少した(Eur Heart J2018;39:26-35.)。
MRAの場合、LVEFが50%以上の患者よりもLVEFが41~49%の患者の方が治療効果が大きい可能性が高い(Circulation2005;112:3738-44.)。
LVEFが60%未満の場合に、サクビトリル/バルサルタンは有用(Eur Heart J. 2023 Aug 14;44(31):2982-2993.)。
その他の薬剤
以下の薬剤は4つの薬を使用した上で使用を検討する薬剤である。
<イバブラジン>
イバブラジンは、洞結節の心臓ペースメーカー電流 I(f) の原因となるチャネルを阻害する。
SHIFT (Systolic Heart failure treatment with the If inhibitor ivabradine Trial)では、洞調律で心拍数が70bpm以上のHFrEF患者6558名を対象に、心血管死と心不全による入院の複合アウトカムがプラセボと比較して18%相対的に減少した(HR 0.82、0.75~0.90)。
<ベルイシグアト>
ベルシグアトは、可溶性グアニル酸シクラーゼを刺激し、一酸化窒素シグナル伝達経路を増強して血管拡張を促進し、心臓リモデリングを軽減する新しい心不全治療薬である。
VICTORIA trialでは、最近入院した、または静脈利尿薬を投与されたHFrEF患者5050名が、プラセボと比較して、ベルシグアトで治療したところ、心血管疾患による死亡または心不全による入院のリスクが10%相対的に減少した(HR0.83~0.98)。
<鉄剤>
内服ではなく、静脈内鉄投与により、HFrEF患者の心不全による入院リスクが軽減され、健康状態が改善されることが示されている。
<GLP1RA>
肥満およびHFpEF患者におけるGLP1RAの使用は薦められているが、HFrEF患者では心不全による入院が増加した。
デバイスと侵襲的治療
<ICD>
複数の試験で、HFrEF患者に対するICD療法の延命効果が実証されているが、最近のDANISH trialでは、非虚血性心筋症患者556人の全死亡率に有意な低下は認められなかった(HR 0.87、0.68~1.12)。しかしながら、70歳未満の患者では、ICDによる延命効果が認められた。しかしこれは、ICDが心臓突然死のみを防ぐという事実を反映している可能性が高く、患者の価値観やADLなどによって意思決定されるべきであろう。
<CRT>
CRTは、QRSが広い患者(通常は左脚ブロックパターンで150ms以上)に最も効果的である。CRTは伝統的に両心室ペーシングに依存してきた。伝導系ペーシングは、ヒス束または左脚をペーシングする新しいアプローチである。小規模な研究では、伝導系ペーシングが心室同期を促進するための潜在的な代替手段となる可能性があることが示唆されている。
<僧帽弁transcatheter edge-to-edge repair(TEER)>
614人の患者を対象としたCOAPT(心不全患者に対するMitraClip経皮的治療の心血管アウトカム評価)試験では、僧帽弁TEERにより心不全による入院が47%減少し(HR0.53、0.40~0.70)、全死亡率が38%減少した(0.62、0.46~0.82)。しかし、MITRA-FR(重度の機能的/二次性僧帽弁逆流症に対するMitraClipデバイスによる経皮的修復)試験では、僧帽弁TEERを伴う心不全による死亡率や入院率の減少は見られなかった(患者304人、OR1.16、0.73~1.84)。
この結果の不一致は、心筋症の重症度とMRの程度が関連していると思われるが、LVDの程度とMRの程度が関連している場合、MVRの恩恵を受けやすくなると考えられる。
<CABG>
STICH trialでは、EF35%以下の1212 人を、CABG or 薬物療法のいずれかに無作為に割り付けた。主要アウトカムである全死因死亡率は、CABGでは有意に低下しなかった (HR 0.86、0.72~1.04)。ただし、副次アウトカムである心血管疾患による死亡または心不全による入院はCABGで改善が見られ (HR 0.74、0.64~0.85)、現在のガイドラインでは、バイパス手術に適した重篤な疾患があり、LVEFが35%未満の場合はバイパス手術が推奨されている。
<PCI>
REVIVED trialでは、左室機能障害を有する虚血性心臓病の患者に対して、PCIによる血行再建術と至適薬物治療単独とを比較した。薬物治療と比較して、PCIによって死亡率や入院率が改善されなかった (HR0.99、0.78~1.27)。
<心臓移植>
心臓移植は、ステージ D の心不全患者の治療の要である。
心臓移植後の平均生存期間は、現在 12 年を超えている。
C型肝炎陽性ドナーからの心臓移植が可能になったことで、潜在的なドナーが増加した。
非薬物・非デバイス治療
<Na制限>
SODIUM-HF trialでは、806人の患者を1日1500mg未満の低ナトリウム食または通常のケアに無作為に割り付けた。心血管疾患による入院、心血管疾患による救急外来受診、全死亡率は同程度であった (HR 0.89、0.63~1.26)。しかしながら、低ナトリウム食を摂った患者は、患者が報告した健康状態が高かった。
ナトリウム制限は患者の予後改善にはつながらないため、他の治療が優先されるべきである。
<水分制限>
6 つの試験のメタ分析では、水分を自由に摂取しても、心不全による再入院や全死亡率は増加しないことが判明した。
まとめ
HFrEF患者では、4剤の治療薬をしっかりと導入することが重要ですね。HFpEFではSGLT2iの導入のみがエビデンスがあります。
他、水分制限、Na制限の有用性について現時点ではあまりエビデンスがないことは知らなかったので、今後の研究には注目して行きたいですね。



コメント