- Eur Heart J. 2024 May 21;45(19):1701-1715.
- doi: 10.1093/eurheartj/ehae150.
- PMID: 38685132
ESCからESUSに関するコンセンサスが出ていたのでまとめます
Introduction
虚血性脳卒中の6人に1人は原因不明の塞栓性脳卒中(ESUS)である。ESUSの定義については以下のFigureの通り。ESUSは複数の潜在的な原因がありどれが実際の塞栓源であるか判断が難しい時がある。

ESUS患者の心血管リスクは高く、5年累積脳卒中再発および心血管イベント発生率は29%, 38%である。
ESUSにおける塞栓リスク評価は以下の通りである。
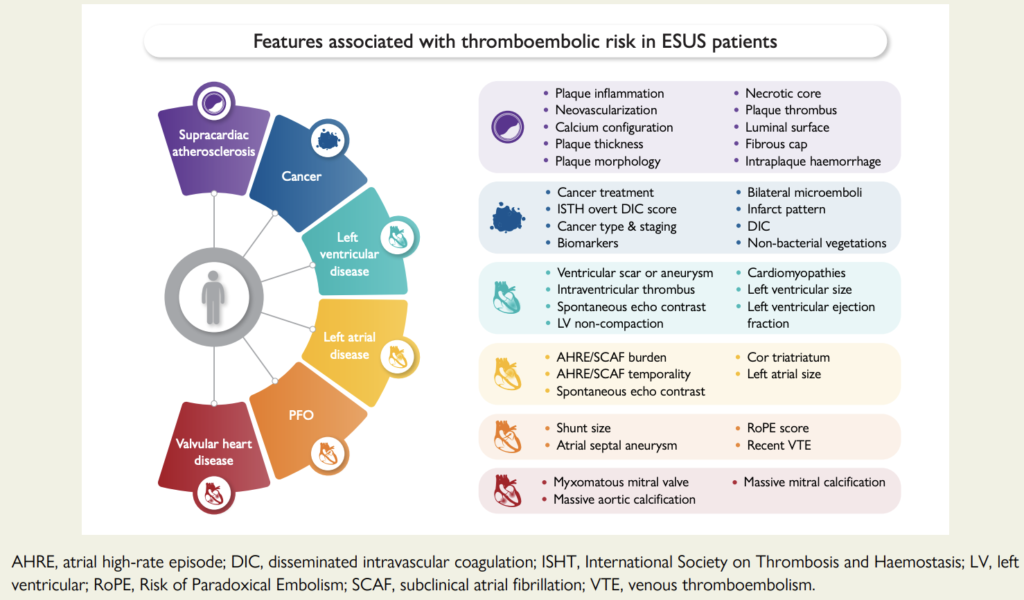
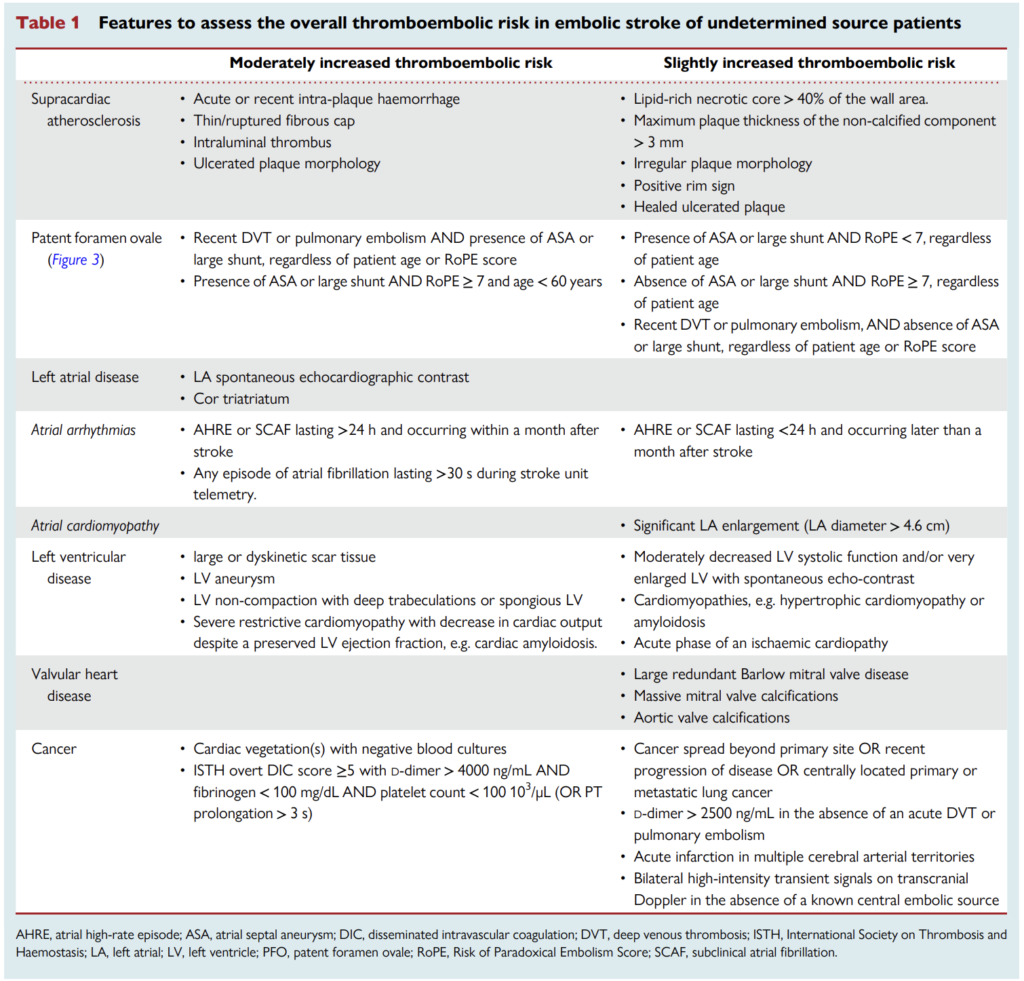
これを以下のように視覚化するとわかりやすい。
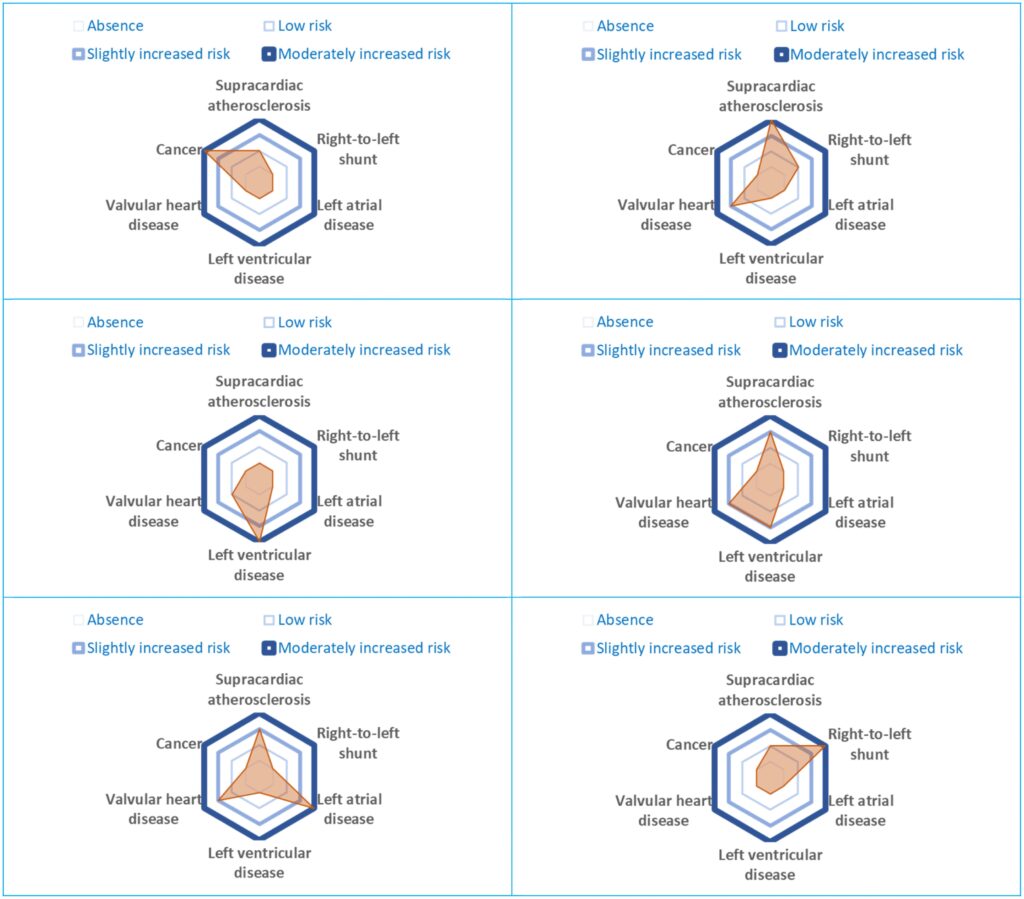
Supracardiac atherosclerosis 心臓より上部の動脈硬化
頸動脈狭窄があるが以下のような状態によって評価される。
★プラーク内出血(Intra-plaque haemorrhage: IPH)
アテローム性プラーク内に血液成分が蓄積すること。プラーク脆弱化の最も重要な特徴である。狭窄が<50%では、同側脳卒中の年間発生率はIPHあれば9%、なければ0.7%であった(JACC Cardiovasc Imaging2020;13:395–406.)。MRIでacute(<1週間)、recent(1-6週)、old(>6週)に分類できる。acuteは脳血管イベントリスク高い。
★Fibrous cap (FC)
プラークの核と動脈内腔を隔てる線維性結合組織の層であり、プラークの脆弱性を評価するもう 1 つの特徴であり、MRI で評価することが望ましい。薄く破裂したFCが脳血管イベントと関連している。
★頸動脈内血栓 (intraluminal thrombus)
頸動脈起源脳卒中の最も強力な予測因子は頸動脈内血栓であり、ついでIPHとなっている。
★頸動脈プラークの内腔面
平滑(smooth)、不規則(irregular)、潰瘍(ulcerated)に分類される。潰瘍面は幅が1mmを超える内膜欠損であり、アテローム性プラークの壊死核が露出している状態である。この状態は脳血管イベント関連あり。
★脂質に富む壊死核(lipid-rich necrotic core: LRNC)
コレステロール結晶、アポトーシス細胞の破片、カルシウム粒子などで構成される不均一な組織である。MRIで、プラークの進行と脆弱性の評価が必要である。LRNCが壁面積の40%を超えるとFC破裂を起こしやすい。
★プラークの厚さ(maximum plaque thickness: MPT)
非石灰化成分の>3mmのプラークの厚さは、同側の脳卒中患者の35%で認め、15%で対側に認める。狭窄の程度よりもMPTが脳虚血症状と関連がある。
★カルシウム
カルシウムの存在がどうかは議論の余地があるが、石灰の大きさ、形状、位置がプラークの発達に影響を与えうる。CTAで、最大厚さが2mm以上の内部lowのプラークを伴う薄い(<2mm)外膜石灰化として定義される、positive rim signはIPHの存在と関連している。
Patent foramen ovale and other right-to-left shunts 卵円孔開存とその他の右左シャント
最も一般的な右左シャントは PFO ですが、他の中隔欠損や肺内シャントなどの他の病態が存在する場合もある。
PFOは経皮的閉鎖により脳卒中リスク軽減できるし、薬物療法と比較してもHR0.41(95%CI 0.28-0.6)であった(JAMA. 2021;326:2277-2286.)。
経皮的閉鎖の有効性に関して、PASCAL分類で、probablyではHR0.1(95%CI 0.03-0.35)、possiblyではHR0.38(95%Cl 0.22-0.65)であったが、relation unlikelyでは利点がなかった(JAMA Neurol. 2020;77:878-886.)。
PASCAL分類はこちら(https://pfo-council.jp/docs/publications/guidance_02_240328.pdfから引用)。
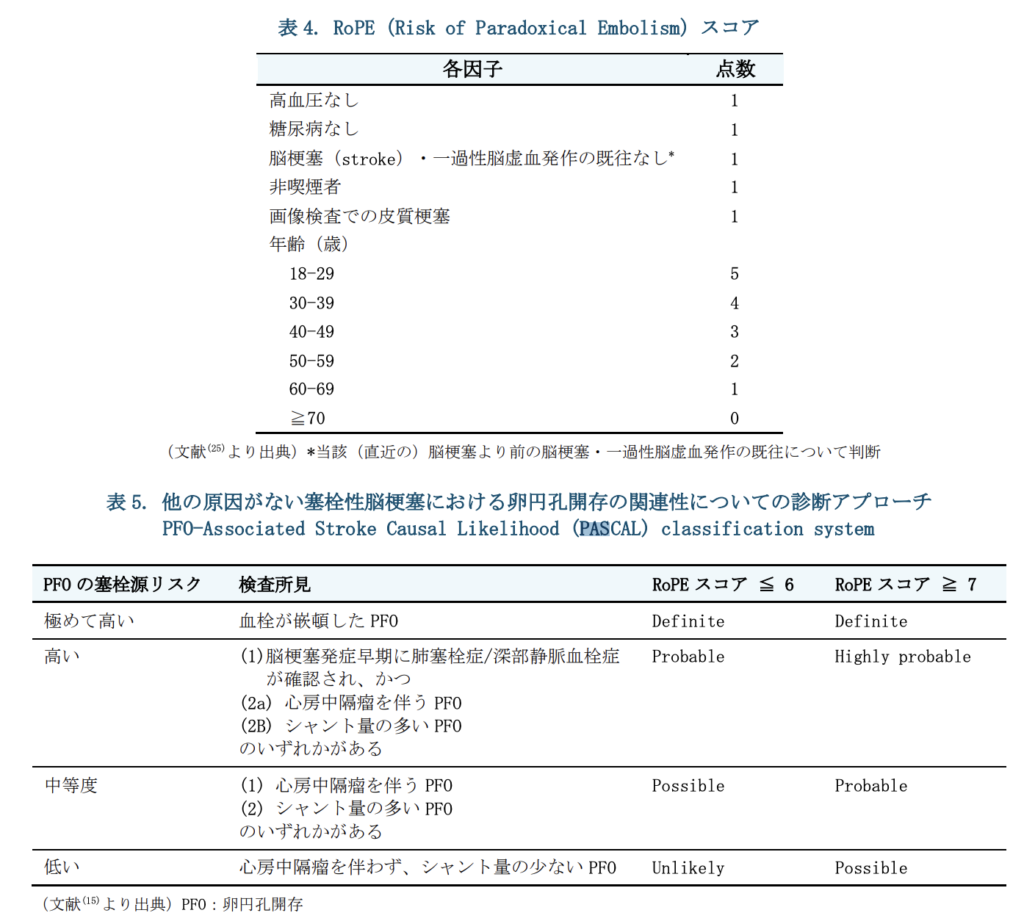
Left atrial disease 左房の疾患
左房や左心耳に血栓が存在すると塞栓リスクが高くなる。抗凝固療法を受けているAF患者における血栓発生率は3%であり、発作性(1%)よりも、非発作性(4.8%)で多い(J Am Coll Cardiol2021;77:2875–86.)。抗凝固療法を受けていないと9%である(J Cardiovasc Electrophysiol2021;32:2179–88.)。
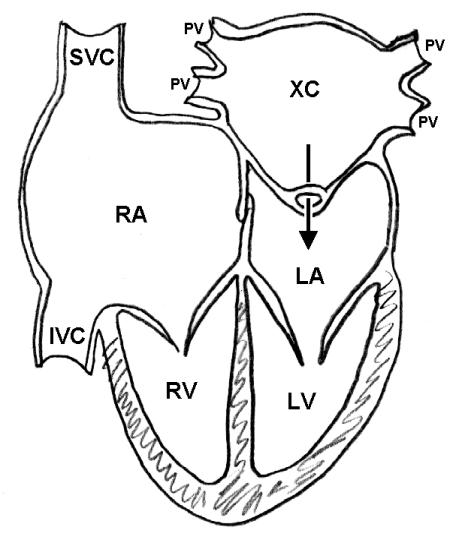
Cor triatriatum sinistrumは先天性心疾患で左房が膜によって2つの部屋に分かれている。ESUSで見つけた場合は脳卒中の原因として考えられる。
- Atrial arrhythmias 心房の不整脈
subclinical AF(SCAF)/atrial high rate episode(AHRE)とESUSの関係は、エピソードが24時間以上続く場合は、脳卒中や全身塞栓症と関連している(Eur Heart J. 2017;38:1339-1344.)。
ただしこれらの患者に対して、抗凝固薬を投与すると、虚血性脳卒中は低下したが(RR0.68 95%CI 0.5-0.92)、major bleedingが増えた(RR1.62, 95%CI 1.05-2.5)。
- Atrial cardiomyopathy 心房心筋症
左房の大きさはAFおよび脳卒中のリスクと関連している。左房の拡大は、加齢に伴う進行性リモデリング、圧力および容量負荷による伸張、酸化ストレスおよび炎症と関連している可能性があり、不整脈および血栓形成環境を形成しうる。リバロキサバンはESUSおよび左房>4.6cmの患者における再発性脳卒中のリスク低下と関連している(JAMA Neurol. 2019;76:764-773.)。
Left ventricular disease 左室疾患
虚血性心疾患やDCM(HFrEF)はは脳卒中を引き起こす可能性がある。EF30%未満はESUSに分類されない。
洞調律でEF低下した患者に対する抗凝固薬はワーファリンと比較して虚血性脳卒中の発症は低下したが(OR0.57, 95%CI 0.44-0.73)、major bleedingは増加した(OR1.92, 95%CI 1.47-2.5)。
心アミロイドーシスはEFが保たれるにもかかわらず、Cardiac outputが低下し左室や左房に血栓が生じる。
LV non-compaction cardiomyopathyや以前に塞栓イベントがあった場合では、抗凝固薬が推奨される。
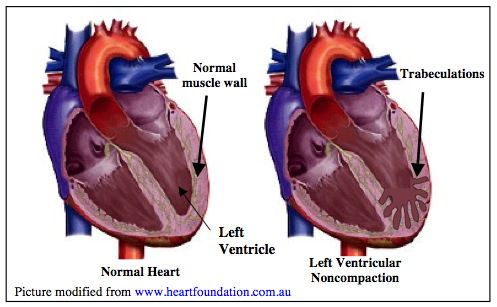
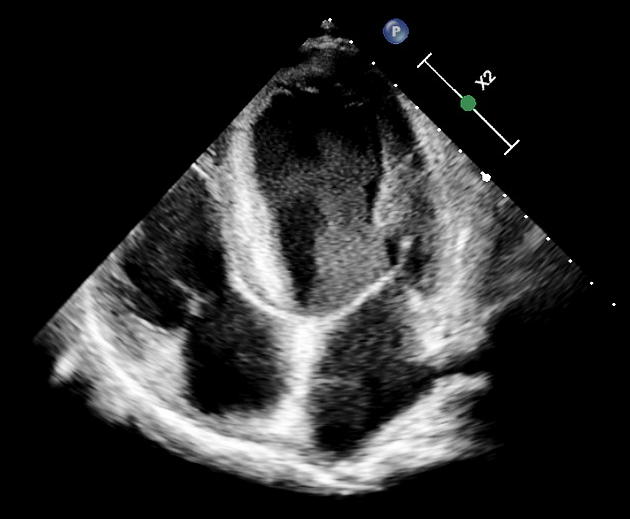
Left ventricular spontaneous echo-contrastは、cardiac outputが低下している患者で見られ、血栓や塞栓と関連がある。
Valvular heart disease 弁膜症疾患
心内膜炎、心臓腫瘍以外の弁膜症で、塞栓症を起こすことは稀である。
しかし、高度な粘液腫性僧帽弁と重度の弁石灰化(大動脈弁や僧帽弁後尖など)は、塞栓リスク増加となる。
ランブル疣贅とは、僧帽弁や大動脈弁に見られる細い糸状の可動する構造物であるが、ESUSとは関連がないということとなっている。
Cancer 腫瘍
非細菌性血栓性心内膜炎(NBTE)や血管内凝固などの凝固亢進プロセス、腫瘍塞栓や腫瘍による圧迫などの直接的な血管損傷、放射線血管障害や化学療法誘発性心筋症などの治療合併症など、いくつかのメカニズムを通じて虚血性脳卒中を引き起こす可能性がある。
がんと診断される150日前から、虚血性脳卒中のリスクは59%増加する( Blood. 2019;133:781-789.)。反対に、虚血性脳卒中患者の2~10%が翌年にがんと診断される。
血栓塞栓症のリスク増加に関連する癌の種類としては、肺、膵臓、胃、大腸、卵巣、膀胱、非ホジキンリンパ腫などがある。
まとめ
まだまだESUSにはわかっていないことがたくさんあり、その治療についてもエビデンスの高いものは少ないです。ただ、しっかりと精査しリスクを評価しながら抗凝固薬、抗血小板薬、脂質コントロールなどを個別の患者に適応していく、しか現状はないと思います。





コメント