Neuroleptic Malignant Syndrome
- N Engl J Med 2024;391:1130-1138
- DOI: 10.1056/NEJMra2404606
悪性症候群に関するレビューです!
疫学
悪性症候群は、関与する薬剤に曝露された患者の0.02~3%に発症すると推定されている。
神経遮断性悪性症候群は、ドパミン遮断薬、特に抗精神病薬にさらされた後の発熱、筋硬直、自律神経失調を特徴とする。
治療は経験的なもので、筋弛緩剤を投与し、通常は集中治療室で厳重に監視する。
再曝露後の再発リスクは低いが、若干のリスクは残る。
臨床症状
精神障害の診断と統計マニュアル』第5版では、神経遮断性悪性症候群の診断基準として、
・ドパミン遮断薬への曝露
・重度の筋強剛
・発熱
および以下の特徴のうち少なくとも2つを挙げている。
・発汗、嚥下障害、振戦、失禁、意識レベルの変化、緘黙、頻脈、血圧上昇または変動性血圧、白血球増加、血清CK値の上昇
悪性症候群の典型的な症状は、自律神経失調症(特に頻脈と急速に変動する高血圧または低血圧、40℃以上への体温上昇、型では緊張病となるようなせん妄、筋緊張亢進)である。血圧変動と筋緊張亢進は通常、本疾患の最初の徴候である。筋強剛はさまざまな表現があるが、基本的には錐体外路性の「鉛管」徴候であり、検査者は四肢の受動運動範囲を通して運動に対する一様な抵抗として認識し、痙縮、ジストニア、痙攣とは区別できる。硬直は第一世代薬剤よりも第二世代薬剤の方が少ないとされる。
強度の硬直は横紋筋融解症、血清CK値の大幅な上昇、腎不全を引き起こすことがある。白血球増多は一般的である。パーキンソン病などの錐体外路系疾患における重度の硬直が、この程度の筋損傷を引き起こすことはまれであるが、これはおそらく、これらの疾患における硬直が神経遮断性悪性症候群における硬直よりも軽度であり、高体温を伴わないためであろう。
薬物曝露から症状発現までの間隔の中央値は4日、罹病期間の中央値は9日であったが、薬物曝露後1日以内に発症した症例もあれば、30日以上経過してから発症した症例もある。
悪性症候群に遭遇する頻度は、薬剤誘発性パーキンソニズムよりもはるかに低い。抗精神病薬に曝露された患者の30%に、硬直やジストニアを伴うパーキンソン症状が発現すると推定されており、これらの所見は初期の悪性症候群と間違われる可能性がある。
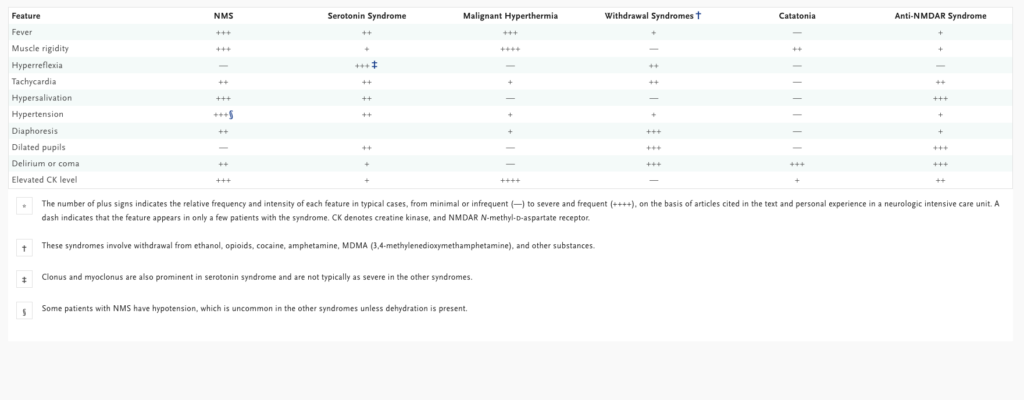
熱中症、離脱症候群、およびアンフェタミン、コカイン、MDMA(3,4-メチレンジオキシメタンフェタミン)、フェンサイクリジンなどの娯楽用乱用薬物による急性中毒は、神経遮断性悪性症候群に類似して見える。また、バクロフェンなどの筋弛緩薬を突然中止すると、神経遮断性悪性症候群の特徴を模倣した筋硬直や精神変化を起こすことがある。
治療
上気道筋、呼吸筋、横隔膜の硬直から急性呼吸困難を呈することがある。さらに、咳嗽が効果的でないため、分泌物や胃内容物を誤嚥することもある。場合によっては挿管および人工呼吸が必要となる。顕著な唾液漏がみられることがあるが、抗コリン薬で対処できる。
ほとんどの患者で血圧変動を伴う頻脈がみられ、若年者では許容される有害事象かもしれないが、冠動脈疾患患者ではtype 2 MIや血清トロポニン値の上昇を誘発する可能性がある。神経遮断薬が心筋を直接損傷するかどうかは不明である。
患者は昏迷し無言になることもあれば、興奮し錯乱状態になることもあるし、せん妄状態になることがある。鎮静・催眠・抗不安作用を有する選択的短時間作用型α2-アドレナリン作動薬であるデクスメデトミジンを投与することで制御できうる。
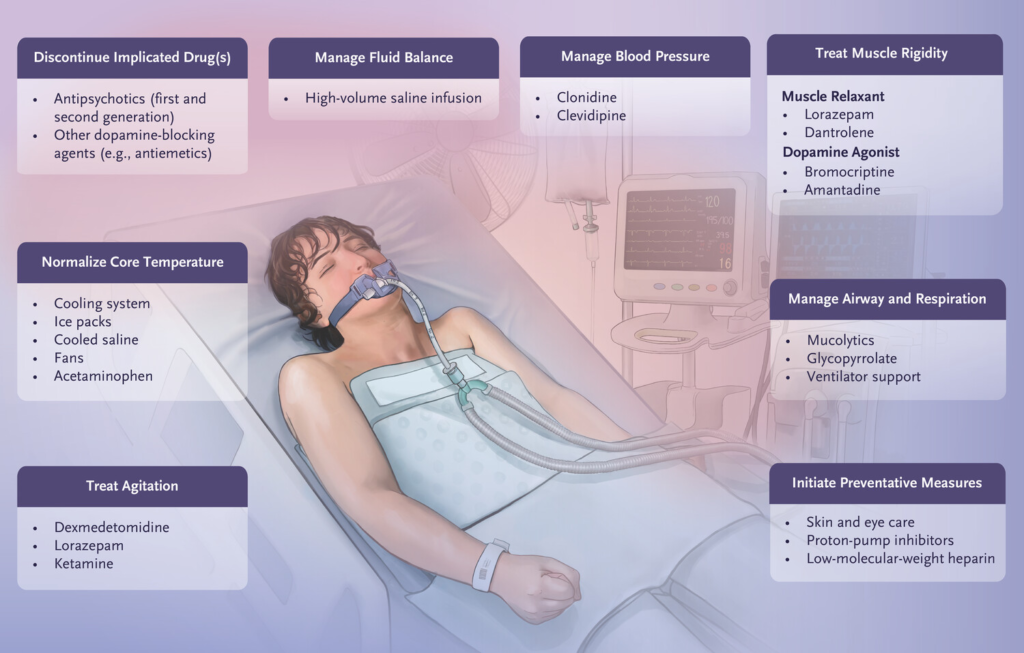
重症例では、低カルシウム血症、低マグネシウム血症、低ナトリウム血症および高ナトリウム血症、高カリウム血症、代謝性アシドーシスを引き起こし、これらはすべて是正が必要である。
血清LDH、ALP、肝酵素の異常値はよくみられるが、一過性である。
発熱を認め、脱水状態となり、硬直により血清CK値が10000以上と高値となることが多い。初期にはCKがそこまで高くないこともあり注意が必要である。
横紋筋融解症を管理するために、大量の静脈内輸液が必要な場合があり、尿量は約200~300ml/hrを目標とする。横紋筋融解症の一般的な合併症である低カルシウム血症は、損傷した筋細胞へのカルシウムの侵入および壊死した筋内でのリン酸カルシウムの沈殿から生じる。例外的に、重度の局所横紋筋融解症はコンパートメント症候群を引き起こし、筋膜切開術を必要とする。高体温症は、アセトアミノフェン1000mgを6時間ごとに経口投与するなどの解熱剤と、ミストや扇風機による蒸発冷却、またはより効率的な体表面温度調節で治療する。
重症例では、高体温、頻脈、高度の血圧不安定に対して、α1アドレナリン受容体の作動薬であるクロニジンや、クレビジピンやニカルジピンなどのカルシウム拮抗薬を必要とする。
ロラゼパムは軽症例では筋弛緩を起こす。悪性症候群の筋徴候が持続または悪化する場合は、筋小胞体でのカルシウム放出を阻害する直接作用型の骨格筋弛緩薬であるダントロレンを投与する。硬直を軽減し、中枢の体温調節領域に対する作用により、ダントロレンは高体温を緩和し、血清CKの上昇を抑制する。高用量投与には肝毒性作用のリスクがあり、一般に肝機能のモニターが必要である。ブロモクリプチンまたはアマンタジンが代替薬として提案されている。どちらも抗精神病薬のドパミン拮抗薬に取って代わるドパミン作動薬であり、短期的な副作用はほとんどない。生命を脅かすような症例では、電気けいれん療法(ECT)が有効であることが報告されているが、他の治療に反応しない患者に限られる。
神経遮断薬性悪性症候群の徴候の評価を混乱させる徴候の発生を避けるために、リチウム、抗コリン療法、セロトニン作動性薬剤などの他の向精神薬も、可能であれば通常は中止する。長時間作用型の注射剤の場合、放出が長期にわたるため、抗精神病薬の作用を即座に除去することは不可能である。一部の抗精神病薬では、薬物の血中濃度が検出されなくなるまで最大60日の間隔が必要である。短時間作用型の経口抗精神病薬の場合、一般に3~5日以内に自然に血清レベルが低下する。
予後、経過
回復に要する時間は様々であるが、一般に7~11日である。支持療法では平均15日であるのに対し、ダントロレンでは9日、ブロモクリプチンでは10日である。回復期間が長引くと、人工呼吸器関連肺炎や敗血症のリスクが高まる。抗精神病薬による治療を再開すると、悪性症候群が再発する可能性があり、最初の曝露から2年後まで続くと報告されている。
再発を予防するためのもう1つの提案は、抗精神病薬の初期用量を少なく投与し、ゆっくりと上方調節することである。クロザピンを含む非定型抗精神病薬への切り替えは、必ずしも神経遮断性悪性症候群の再発を予防するとは限らないが、重度または致死的な再発のリスクは低いかもしれない。
まとめ
悪性症候群に対する治療としては、ロラゼパム、ダントロレン、ブロモクリプチン、アマンタジン、ECTなどがありますね。全身状態管理しながら上記薬剤を使用してコントロールしていく必要があります。









コメント